Liste des éléments
»
Actinium
»
Argent
»
Argon
»
Arsenic
»
Astate
»
Azote
»
Baryum
»
Bismuth
»
Bohrium
»
Bore
»
Brome
»
Cadmium
»
Calcium
»
Carbone
»
Cérium
»
Césium
»
Chlore
»
Chrome
»
Cobalt
»
Cuivre
»
Curium
»
Dubnium
»
Erbium
»
Etain
»
Europium
»
Fer
»
Fermium
»
Fluor
»
Francium
»
Gallium
»
Hafnium
»
Hassium
»
Hélium
»
Holmium
»
Indium
»
Iode
»
Iridium
»
Krypton
»
Lanthane
»
Lithium
»
Lutécium
»
Mercure
»
Néodyme
»
Néon
»
Nickel
»
Nihonium
»
Niobium
»
Nobélium
»
Or
»
Osmium
»
Oxygène
»
Platine
»
Plomb
»
Polonium
»
Radium
»
Radon
»
Rhénium
»
Rhodium
»
Rubidium
»
Samarium
»
Scandium
»
Sélénium
»
Silicium
»
Sodium
»
Soufre
»
Tantale
»
Tellure
»
Tennesse
»
Terbium
»
Thallium
»
Thorium
»
Thulium
»
Titane
»
Uranium
»
Vanadium
»
Xénon
»
Yttrium
»
Zinc
C - Carbone - AUTRE NON MÉTAL
Le carbone est un élément chimique essentiel à la vie et à la fabrication de produits de tous genres. Il est représenté par le symbole C et se trouve en abondance dans l'environnement sous forme de carbone organique (comme dans le charbon, les hydrocarbures, etc.) et sous forme inorganique (comme le dioxyde de carbone [CO2], le monoxyde de carbone [CO], etc.). C'est un élément vital à la vie organisée sur Terre.
Le carbone est incolore, inodore et associe à d'autres éléments pour former des composés organiques et inorganiques. Il est considéré comme l'un des trois éléments qui jouent un rôle majeur dans la chimie organique (avec l'hydrogène et l'oxygène). Le carbone se lie à lui-même et à d'autres éléments pour former des molécules dont les propriétés sont déterminées par le type de liaison entre les atomes de carbone.
Le carbone est un élément polyvalent et les molécules qu'il forme peuvent avoir des propriétés variables. Les propriétés les plus importantes avec le carbone sont la conductivité électrique, la résistance thermique et la capacité à absorber l'humidité. Les produits faits à base de carbone sont très utilisés dans l'industrie et dans la vie quotidienne. Les principaux produits à base de carbone sont les carburants, les plastiques, les colorants, les encres, l'acier, les textiles et les produits chimiques pour les cosmétiques et les médicaments.
Le carbone est également un élément important pour la production et le stockage de l'énergie. Le carbone est utilisé pour produire de l'énergie dans les centrales électriques et peut être stocké sous forme de charbon, de gaz naturel et de pétrole. Les combustibles fossiles peuvent être transformés en énergie à partir du carbone qu'ils contiennent. Le carbone peut également être stocké sous forme de biomasse (matière organique végétale ou animale), de gaz carbonique ou de produits chimiques à base de carbone.
Le carbone est incolore, inodore et associe à d'autres éléments pour former des composés organiques et inorganiques. Il est considéré comme l'un des trois éléments qui jouent un rôle majeur dans la chimie organique (avec l'hydrogène et l'oxygène). Le carbone se lie à lui-même et à d'autres éléments pour former des molécules dont les propriétés sont déterminées par le type de liaison entre les atomes de carbone.
Le carbone est un élément polyvalent et les molécules qu'il forme peuvent avoir des propriétés variables. Les propriétés les plus importantes avec le carbone sont la conductivité électrique, la résistance thermique et la capacité à absorber l'humidité. Les produits faits à base de carbone sont très utilisés dans l'industrie et dans la vie quotidienne. Les principaux produits à base de carbone sont les carburants, les plastiques, les colorants, les encres, l'acier, les textiles et les produits chimiques pour les cosmétiques et les médicaments.
Le carbone est également un élément important pour la production et le stockage de l'énergie. Le carbone est utilisé pour produire de l'énergie dans les centrales électriques et peut être stocké sous forme de charbon, de gaz naturel et de pétrole. Les combustibles fossiles peuvent être transformés en énergie à partir du carbone qu'ils contiennent. Le carbone peut également être stocké sous forme de biomasse (matière organique végétale ou animale), de gaz carbonique ou de produits chimiques à base de carbone.
Synthétique
Radioactif
Liquide
Gazeux
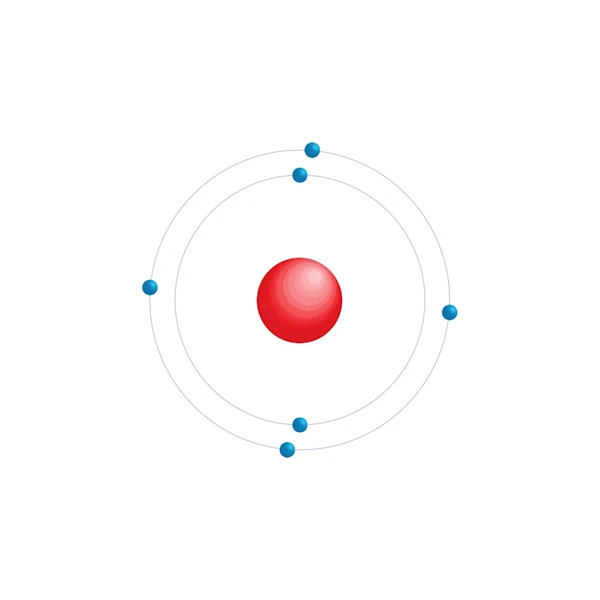
Diagramme de configuration électronique
| Nom | Carbone |
| Numéro atomique | 6 |
| Masse atomique | 12.0112 |
| Symbole | C |
| Point de fusion | 3550 |
| Point d'ébullition | 4827 |
| Densité | 2.267 |
| Période | 2 |
| Groupe | 14 |
| Découverte | 0 Prehistoric |
| Abondance | 200 |
| Radius | 0.91 |
| Electronégativité | 2.55 |
| Ionisation | 11.2603 |
| Nombre d'isotope | 7 |
| Configuration électronqiue | [He] 2s2 2p2 |
| Etats d'oxydation | -4,-3,-2,-1,1,2,3,4 |
| Electron par niveau d'énergie | 2,4 |
| Minéral | Dureté | Densité |
| Abelsonite | 2.00 / 2.50 | 1.45 |
| Abenakiite-(Ce) | 4.00 / 4.00 | 3.21 |
| Acetamide | 1.00 / 1.50 | 1.17 |
| Adamsite-(Y) | 3.00 / 3.00 | |
| Aerinite | 3.00 / 3.00 | 2.48 |
| Afghanite | 5.50 / 6.00 | 2.55 |
| Agaite | 6.99 | |
| Agricolaite | 4.00 / 4.00 | 3.53 |
| Albrechtschraufite | 2.00 / 3.00 | 2.60 |
| Alexkhomyakovite | ||
| Alloriite | 5.00 / 5.00 | 2.35 |
| Alstonite | 4.00 / 4.50 | 3.69 |
| Alumohydrocalcite | 2.50 / 2.50 | 2.23 |
| Ambre | 2.00 / 2.50 | 1.10 |
| Ammonite | 6.00 / 7.00 | 3.20 |
| Ancylite-(Ce) | 4.50 / 4.50 | 3.90 |
| Ancylite-(La) | 4.00 / 4.50 | 3.88 |
| Andersonite | 2.50 / 2.50 | 2.79 |
| Ankerite | 3.50 / 4.00 | 3.00 |
| Antipinite | 2.00 / 2.00 | 2.55 |
| Aragonite | 3.50 / 4.00 | 2.93 |
| Arisite-(Ce) | ||
| Arisite-(La) | 3.00 / 3.50 | 4.07 |
| Armangite | 4.00 / 4.00 | 4.43 |
| Artinite | 2.50 / 2.50 | 2.00 |
| Ashburtonite | 4.69 | |
| Ashcroftine-(Y) | 5.00 / 5.00 | 2.61 |
| Astrocyanite-(Ce) | 2.00 / 3.00 | 3.80 |
| Aurichalcite | 2.00 / 2.00 | 3.64 |
| Azurite | 3.50 / 4.00 | 3.77 |
| Balliranoite | ||
| Barbertonite | 1.50 / 2.00 | 2.10 |
| Barentsite | 3.00 / 3.00 | 2.56 |
| Barringtonite | 2.83 | |
| Barstowite | 3.00 / 3.00 | 5.50 |
| Barytocalcite | 4.00 / 4.00 | 3.64 |
| Bastnäsite-(Ce) | 4.00 / 5.00 | 4.95 |
| Bastnäsite-(La) | 4.00 / 5.00 | 4.95 |
| Bastnäsite-(Nd) | 4.00 / 4.50 | 5.23 |
| Bastnäsite-(Y) | 4.00 / 4.50 | 4.90 |
| Bayleyite | 2.05 | |
| Baylissite | 2.00 | |
| Benstonite | 3.00 / 4.00 | 3.60 |
| Beyerite | 2.00 / 3.00 | 6.56 |
| Bijvoetite-(Y) | 2.00 / 2.00 | 3.90 |
| Biraite-(Ce) | 5.00 / 5.00 | 4.76 |
| Birunite | 2.00 / 2.00 | 2.36 |
| Bismutite | 4.00 / 4.00 | 7.00 |
| Blatonite | 2.00 / 3.00 | 3.99 |
| Bonshtedtite | 4.00 / 4.00 | 2.95 |
| Borcarite | 4.00 / 4.00 | 2.77 |
| Bosoite | ||
| Bradleyite | 3.00 / 4.00 | 2.73 |
| Braunerite | ||
| Brenkite | 3.10 | |
| Brianyoungite | 2.00 / 2.50 | 3.93 |
| Britvinite | 3.00 / 3.00 | 5.51 |
| Brugnatellite | 2.00 / 2.00 | 2.14 |
| Burbankite | 3.50 / 3.50 | 3.50 |
| Burkeite | 3.50 / 3.50 | 2.57 |
| Bussenite | 4.00 / 4.00 | 3.63 |
| Bütschliite | 2.00 | |
| Calcioancylite-(Ce) | 4.00 / 4.50 | |
| Calcioancylite-(Nd) | 4.00 / 4.50 | |
| Calcioburbankite | 3.00 / 4.00 | 3.45 |
| Calcite | 3.00 / 3.00 | 2.71 |
| Calclacite | 1.00 | |
| Caledonite | 2.50 / 3.00 | 5.70 |
| Calkinsite-(Ce) | 2.50 / 2.50 | 3.27 |
| Callaghanite | 3.00 / 3.50 | 2.71 |
| Camérolaite | 3.10 | |
| Canavesite | 1.80 | |
| Cancrinite | 6.00 / 6.00 | 2.40 |
| Cancrisilite | 5.00 / 5.00 | 2.40 |
| Caoxite | 2.00 / 2.50 | 1.85 |
| Carboborite | 2.00 / 2.00 | 2.12 |
| Carbobystrite | 6.00 / 6.00 | 2.37 |
| Carbocernaite | 3.00 / 3.00 | 3.53 |
| Carbokentbrooksite | 5.00 / 5.00 | 3.14 |
| Carbonate-fluorapatite | 5.00 / 5.00 | 3.12 |
| Carbonate-hydroxylapatite | 5.00 / 5.00 | 3.00 |
| Carbonatecyanotrichite | 2.00 / 2.00 | 2.65 |
| Carborandite | ||
| Caresite | 2.00 / 2.00 | 2.57 |
| Carletonite | 4.00 / 4.50 | 2.45 |
| Carpathite | 1.50 / 1.50 | 1.29 |
| Carraraite | ||
| Carrboydite | 2.50 | |
| Caysichite-(Y) | 4.50 / 4.50 | 3.03 |
| Cebaite-(Ce) | 4.50 / 5.00 | 4.81 |
| Cebaite-(Nd) | 4.50 / 5.00 | 4.80 |
| Cejkaite | 3.67 | |
| Cérusite | 3.00 / 3.50 | 6.50 |
| Chalconatronite | 1.00 / 2.00 | 2.27 |
| Chanabayaite | 2.00 / 2.00 | 1.46 |
| Chaoite | 1.00 / 2.00 | 3.33 |
| Charmarite | ||
| Chibaite | 6.50 / 7.00 | 1.93 |
| Chlorartinite | 1.87 |
 mineraly.fr
mineraly.fr
 mineraly.co.uk
mineraly.co.uk
 mineraly.com.de
mineraly.com.de
 mineraly.it
mineraly.it
 mineraly.es
mineraly.es
 mineraly.nl
mineraly.nl
 mineraly.pt
mineraly.pt
 mineraly.se
mineraly.se