Liste des éléments
»
Actinium
»
Argent
»
Argon
»
Arsenic
»
Astate
»
Azote
»
Baryum
»
Bismuth
»
Bohrium
»
Bore
»
Brome
»
Cadmium
»
Calcium
»
Carbone
»
Cérium
»
Césium
»
Chlore
»
Chrome
»
Cobalt
»
Cuivre
»
Curium
»
Dubnium
»
Erbium
»
Etain
»
Europium
»
Fer
»
Fermium
»
Fluor
»
Francium
»
Gallium
»
Hafnium
»
Hassium
»
Hélium
»
Holmium
»
Indium
»
Iode
»
Iridium
»
Krypton
»
Lanthane
»
Lithium
»
Lutécium
»
Mercure
»
Néodyme
»
Néon
»
Nickel
»
Nihonium
»
Niobium
»
Nobélium
»
Or
»
Osmium
»
Oxygène
»
Platine
»
Plomb
»
Polonium
»
Radium
»
Radon
»
Rhénium
»
Rhodium
»
Rubidium
»
Samarium
»
Scandium
»
Sélénium
»
Silicium
»
Sodium
»
Soufre
»
Tantale
»
Tellure
»
Tennesse
»
Terbium
»
Thallium
»
Thorium
»
Thulium
»
Titane
»
Uranium
»
Vanadium
»
Xénon
»
Yttrium
»
Zinc
minéralogie
élements
Ds Darmstadtium
Ds - Darmstadtium - NON CLASSÉS
Darmstadtium est un élément chimique de la famille des actinides. Son numéro atomique est le 110 et sa masse atomique approximative est de 281. Il a été découvert en 1994 par des scientifiques allemands à l'Institut Max Planck à Darmstadt.
La forme stable de l'élément est manganèse, mais il est le plus souvent observé dans des états ioniques très instables. Il est produit par fusion nucléaire et n'a jamais été identifié à l'état naturel. L'isotope le plus stable de l'élément est le Darmstadtium-281 qui a une demi-vie d'environ 39 microsecondes.
La grande instabilité du darmstadtium limite les recherches qui peuvent être effectuées sur ses propriétés. On pense cependant que ses propriétés chimiques sont similaires à celles des autres éléments transuraniens. Le darmstadtium peut former des composés oxydés avec des ions hydroxyle et des ions sulfure.
Le darmstadtium n'a pas d'utilisation pratique. Toutefois, sa découverte a été importante pour aider les scientifiques à comprendre les propriétés des éléments chimiques les plus lourds.
La forme stable de l'élément est manganèse, mais il est le plus souvent observé dans des états ioniques très instables. Il est produit par fusion nucléaire et n'a jamais été identifié à l'état naturel. L'isotope le plus stable de l'élément est le Darmstadtium-281 qui a une demi-vie d'environ 39 microsecondes.
La grande instabilité du darmstadtium limite les recherches qui peuvent être effectuées sur ses propriétés. On pense cependant que ses propriétés chimiques sont similaires à celles des autres éléments transuraniens. Le darmstadtium peut former des composés oxydés avec des ions hydroxyle et des ions sulfure.
Le darmstadtium n'a pas d'utilisation pratique. Toutefois, sa découverte a été importante pour aider les scientifiques à comprendre les propriétés des éléments chimiques les plus lourds.
Synthétique
Radioactif
Liquide
Gazeux
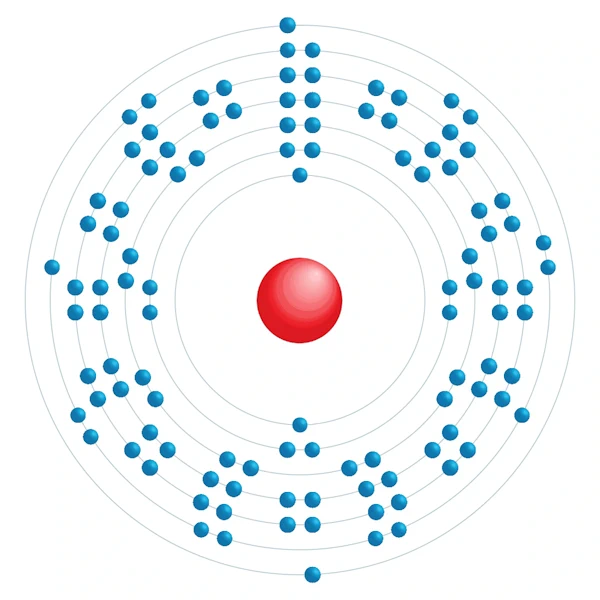
Diagramme de configuration électronique
| Nom | Darmstadtium |
| Numéro atomique | 110 |
| Masse atomique | 281 |
| Symbole | Ds |
| Point de fusion | 0 |
| Point d'ébullition | 0 |
| Densité | 34.8 |
| Période | 7 |
| Groupe | 10 |
| Découverte | 1994 / |
| Abondance | 0 |
| Radius | 0 |
| Electronégativité | 0 |
| Ionisation | 0 |
| Nombre d'isotope | 0 |
| Configuration électronqiue | [Rn] 5f14 6d9 7s1 |
| Etats d'oxydation | 0 |
| Electron par niveau d'énergie | 2,8,18,32,32,16,2 |
 mineraly.fr
mineraly.fr
 mineraly.co.uk
mineraly.co.uk
 mineraly.com.de
mineraly.com.de
 mineraly.it
mineraly.it
 mineraly.es
mineraly.es
 mineraly.nl
mineraly.nl
 mineraly.pt
mineraly.pt
 mineraly.se
mineraly.se