Liste des éléments
»
Actinium
»
Argent
»
Argon
»
Arsenic
»
Astate
»
Azote
»
Baryum
»
Bismuth
»
Bohrium
»
Bore
»
Brome
»
Cadmium
»
Calcium
»
Carbone
»
Cérium
»
Césium
»
Chlore
»
Chrome
»
Cobalt
»
Cuivre
»
Curium
»
Dubnium
»
Erbium
»
Etain
»
Europium
»
Fer
»
Fermium
»
Fluor
»
Francium
»
Gallium
»
Hafnium
»
Hassium
»
Hélium
»
Holmium
»
Indium
»
Iode
»
Iridium
»
Krypton
»
Lanthane
»
Lithium
»
Lutécium
»
Mercure
»
Néodyme
»
Néon
»
Nickel
»
Nihonium
»
Niobium
»
Nobélium
»
Or
»
Osmium
»
Oxygène
»
Platine
»
Plomb
»
Polonium
»
Radium
»
Radon
»
Rhénium
»
Rhodium
»
Rubidium
»
Samarium
»
Scandium
»
Sélénium
»
Silicium
»
Sodium
»
Soufre
»
Tantale
»
Tellure
»
Tennesse
»
Terbium
»
Thallium
»
Thorium
»
Thulium
»
Titane
»
Uranium
»
Vanadium
»
Xénon
»
Yttrium
»
Zinc
minéralogie
élements
Ru Ruthénium
Ru - Ruthénium - MÉTAL DE TRANSITION
Le ruthénium est un élément chimique métallique de numéro atomique 44 et de symbole chimique Ru. Le ruthénium est le 58ème élément le plus abondant dans la croûte terrestre, ce qui en fait un élément relativement rare. Il est un des métaux de transition et est le membre le plus récent de la famille du platine.
Le ruthénium se présente sous forme solide à température ambiante. Il est dur et cassant, à la limite du blanc et se forme généralement sous forme de poudre. Il est légèrement plus lourd que le platine, mais légèrement plus léger que l'iridium.
Le ruthénium possède plusieurs propriétés remarquables. C'est un excellent catalyseur et ses propriétés chimiques sont similaires à celles des autres métaux de transition. Il est très résistant aux acides, mais est vulnérable aux agents de blanchiment et à l'eau oxygénée. Le ruthénium est très réfractaire et peut résister aux températures extrêmes jusqu'à 1700°C.
Le ruthénium a été isolé pour la première fois en 1844 par Karl Klaus, un chimiste russe. Depuis lors, il a été largement utilisé à des fins industrielles. Cet élément est largement utilisé dans la fabrication de catalyseurs et de moteurs à combustion interne, ainsi que pour la fabrication de fils métalliques, de tiges et d'autres produits métalliques. Il est également utilisé pour fabriquer des alliages pour la fabrication de pièces métalliques qui doivent résister à des températures élevées.
Le ruthénium est également utilisé en médecine, notamment pour la fabrication de prothèses dentaires, de couronnes et de ponts. Il est également utilisé pour le traitement des maladies cardiaques et pour traiter certains cancer.
Enfin, le ruthénium est également utilisé dans la fabrication de bijoux et d'objets décoratifs, car il est très difficile de le corroder et qu'il résiste bien à la lumière, à la chaleur et aux produits chimiques.
Le ruthénium se présente sous forme solide à température ambiante. Il est dur et cassant, à la limite du blanc et se forme généralement sous forme de poudre. Il est légèrement plus lourd que le platine, mais légèrement plus léger que l'iridium.
Le ruthénium possède plusieurs propriétés remarquables. C'est un excellent catalyseur et ses propriétés chimiques sont similaires à celles des autres métaux de transition. Il est très résistant aux acides, mais est vulnérable aux agents de blanchiment et à l'eau oxygénée. Le ruthénium est très réfractaire et peut résister aux températures extrêmes jusqu'à 1700°C.
Le ruthénium a été isolé pour la première fois en 1844 par Karl Klaus, un chimiste russe. Depuis lors, il a été largement utilisé à des fins industrielles. Cet élément est largement utilisé dans la fabrication de catalyseurs et de moteurs à combustion interne, ainsi que pour la fabrication de fils métalliques, de tiges et d'autres produits métalliques. Il est également utilisé pour fabriquer des alliages pour la fabrication de pièces métalliques qui doivent résister à des températures élevées.
Le ruthénium est également utilisé en médecine, notamment pour la fabrication de prothèses dentaires, de couronnes et de ponts. Il est également utilisé pour le traitement des maladies cardiaques et pour traiter certains cancer.
Enfin, le ruthénium est également utilisé dans la fabrication de bijoux et d'objets décoratifs, car il est très difficile de le corroder et qu'il résiste bien à la lumière, à la chaleur et aux produits chimiques.
Synthétique
Radioactif
Liquide
Gazeux
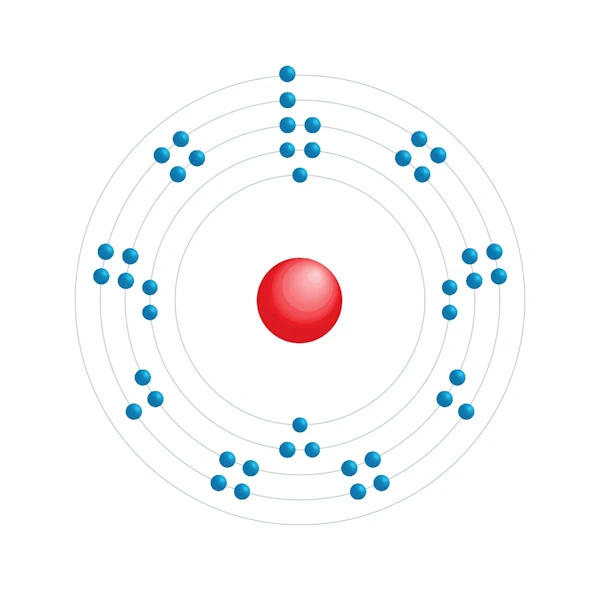
Diagramme de configuration électronique
| Nom | Ruthénium |
| Numéro atomique | 44 |
| Masse atomique | 101.07 |
| Symbole | Ru |
| Point de fusion | 2310 |
| Point d'ébullition | 3900 |
| Densité | 12.37 |
| Période | 5 |
| Groupe | 8 |
| Découverte | 1844 Klaus |
| Abondance | 0.001 |
| Radius | 1.9 |
| Electronégativité | 2.2 |
| Ionisation | 7.3605 |
| Nombre d'isotope | 16 |
| Configuration électronqiue | [Kr] 4d7 5s1 |
| Etats d'oxydation | -2,1,2,3,4,5,6,7,8 |
| Electron par niveau d'énergie | 2,8,18,15,1 |
| Minéral | Dureté | Densité |
| Anduoite | 7.00 / 7.00 | 8.00 |
| Hexaferrum | 6.00 / 7.00 | 10.69 |
| Hexamolybdenum | 11.90 | |
| Irarsite | 6.50 / 6.50 | 11.00 |
| Iridarsenite | 5.00 / 5.50 | 10.90 |
| Iridium | 6.00 / 7.00 | 22.60 |
| Laurite | 7.50 / 7.50 | 6.99 |
| Omeiite | 7.00 / 7.00 | 11.20 |
| Osarsite | 6.00 / 6.00 | 8.44 |
| Platarsite | 7.50 / 7.50 | 8.00 |
| Ruarsite | 6.00 / 7.00 | 7.00 |
| Ruthenarsenite | 6.00 / 6.50 | 10.00 |
| Rutheniridosmine | 6.00 / 7.00 | 21.00 |
| Ruthenium | 6.50 / 6.50 | 12.20 |
 mineraly.fr
mineraly.fr
 mineraly.co.uk
mineraly.co.uk
 mineraly.com.de
mineraly.com.de
 mineraly.it
mineraly.it
 mineraly.es
mineraly.es
 mineraly.nl
mineraly.nl
 mineraly.pt
mineraly.pt
 mineraly.se
mineraly.se